Gsh-Va Glutatione. Radicali liberi e infiammazione
All’inizio dell’ultimo quarto del 20° sec. erano due i fenomeni fisiopatologici che sembravano legati primariamente ai radicali liberi.
Il primo, ampiamente confermato, è la produzione di ROS da parte di cellule specializzate, i macrofagi, come reazione alla presenza di microrganismi o particelle estranei all’organismo, fase iniziale della risposta antinfettiva e infiammatoria in generale.
Il secondo, ancora oggetto di dibattito, è il ruolo, apparentemente paradossale dei ROS, nel danno ischemico o ipossico dei tessuti (comunemente detto infarto) in seguito all’occlusione di un vaso sanguigno.
In ambedue i casi si tratta di interpretazioni tipiche del secolo scorso.
L’approccio attuale è diverso ma comune ai due fenomeni.
I ROS prodotti dai macrofagi attraverso un meccanismo recettoriale che coinvolge un’ossidasi di membrana simile a quella per l’insulina, attivano mediatori molecolari comuni all’infiammazione e a molti stati patologici, soprattutto di natura cardiovascolare, come l’aterosclerosi, l’infarto cardiaco e l’ictus cerebrale, ma anche le malattie neurodegenerative e l’obesità.
Il gruppo sempre più vasto di quelle che possiamo chiamare malattie macrofagiche trova un meccanismo unificante nel ruolo che i ROS hanno nell’attivare l’immunità congenita o innata come risposta a numerosi stress ambientali ed endogeni:
- eccessiva o scorretta alimentazione,
- fumo di sigaretta,
- stress psicologici, tutti fattori notoriamente implicati nelle malattie croniche sopramenzionate.
L’immunità innata è costituita da quei sistemi molecolari e cellulari che nella medicina del 20° sec. erano indicati collettivamente come risposta della fase acuta e che sono messi in campo dall’organismo come prima linea di difesa contro ogni tipo di perturbamento dell’omeostasi: invasioni microbiche o virali, aggressioni da agenti chimici o fisici, stress psicologici e metabolici.
In tutti questi casi i RONS possono essere prodotti:
- dall’agente perturbatore medesimo, come nel caso delle radiazioni;
- dall’ossidasi di membrana del macrofago, come nel caso delle infezioni;
- da metaboliti ossidabili, per es. i neurotrasmettitori (catecolamine) prodotti in eccesso nell’allarme psichico, da sostanze contenute nei cibi (grassi insaturi) o derivate dal metabolismo dei nutrienti (glucosio) in quantità eccessive, da molecole che si accumulano nelle zone infartuate dei tessuti.
I RONS così formati non agiscono solo a livello di danno locale, ma sono registrati da recettori specifici di macrofagi specializzati, presenti anche nel tessuto adiposo e nel tessuto endoteliale, che agiscono come cellule sentinella.
Essi attivano, al loro interno, geni per la sintesi di mediatori proteici deputati alla propagazione della risposta immune.
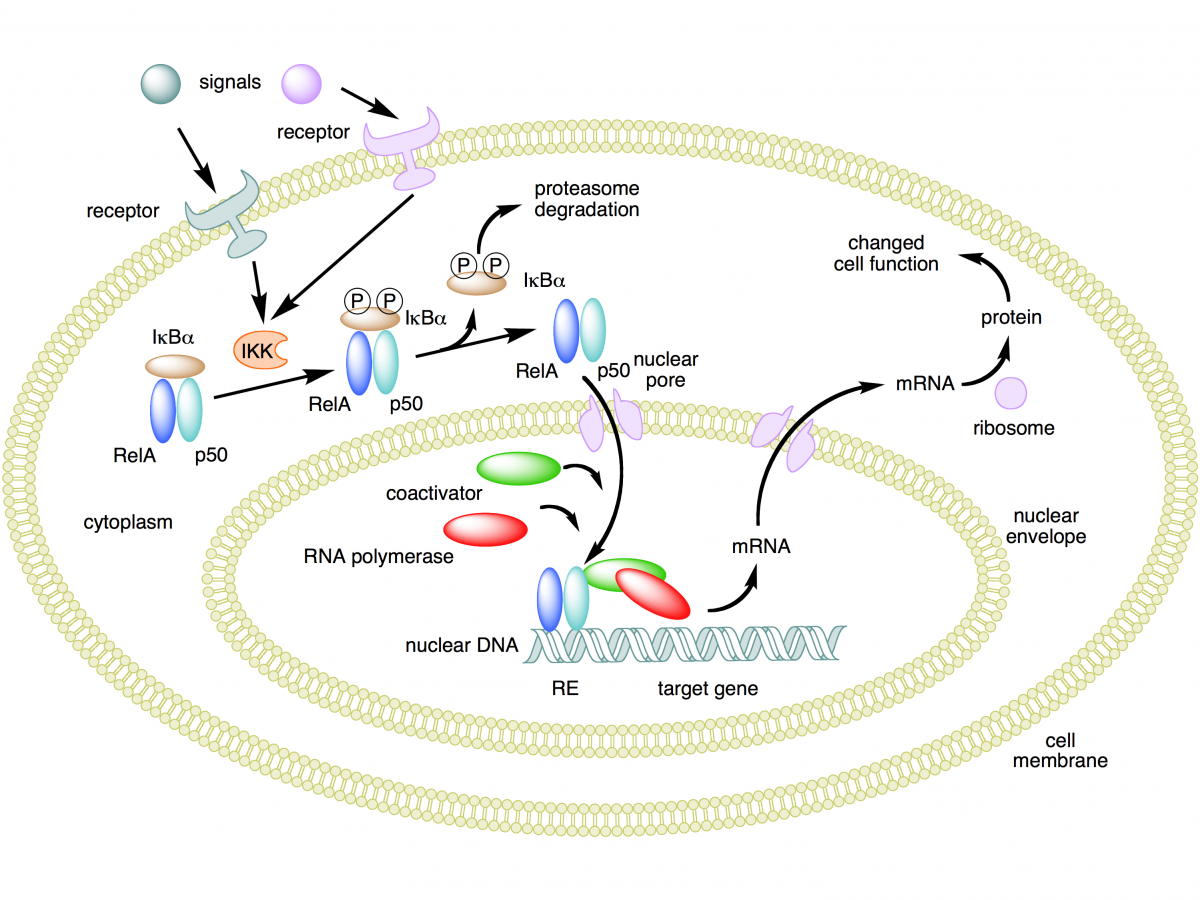
Il primo di questi mediatori si chiama NF-κB e stimola in vari tessuti la produzione di citochine, quali l’interleuchina6 e il fattore di necrosi tumorale, che sono i veri e propri esecutori dei fenomeni infiammatori evoluti per la difesa contro lo stress iniziale, ma che poi, se lo stimolo persiste, diventano il punto di partenza delle malattie croniche più importanti:
- aumentata coagulabilità del sangue, e conseguente rischio di infarto,
- maggiore permeabilità dell’endotelio con predisposizione alle lesioni aterosclerotiche,
- resistenza all’insulina nel tessuto adiposo per rallentare il flusso di glucosio con maggiore probabilità di insorgenza di diabete.
L’attivazione di una risposta di questo tipo è stata riscontrata anche nel cervello dell’anziano e intorno alle lesioni tipiche delle malattie neurodegenerative, come reazione alla produzione anomala di ROS che si ha in queste due situazioni.
Il fatto che la risposta infiammatoria sia la più generale e, quantitativamente, la più imponente fonte di RONS negli organismi è confermato sia dalla presenza di proteine nitrosilate nei tessuti interessati, sia dall’elevata e specifica induzione di superossido dismutasi mitocondriale (SOD2) come ‘contromisura’ all’aumento del loro flusso nella sede più sensibile al controllo dell’omeostasi radicalica.















